PURIFICATION OF WASTE WATER FROM IONS OF HEAVY METALS WITH NATIVE AND MODIFIED SAWDUST OF ACACIA AURICULIFORMIS
ОЧИСТКА СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ НАТИВНЫМИ И МОДИФИЦИРОВАННЫМИ ОПИЛКАМИ АКАЦИИ УШКОВИДНОЙ
JOURNAL: CONSTRUCTION ECONOMIC AND ENVIRONMENTAL MANAGEMENT Volume № 1-2 (82-83), 2022
Section 5. Regional problems of environmental management
Publication text (PDF): Download
UDK: 628.3
AUTHOR AND PUBLICATION INFORMATION
AUTHORS:
- Nguyen T.K.T., Vietchi Industrial University; Vietchi, Vietnam
- Galimova R.Z., Kazan National Research Technological University, Kazan, Russia
- Dryakhlov V.O. Kazan National Research Technological University, Kazan, Russia
- Shaikhiev I.G., Kazan National Research Technological University, Kazan, Russia
- Sverguzova S.V., Belgorod State Technological University named after V.G. Shukhov, Belgorod, Russia
- Voronina Y.S., Belgorod State Technological University named after V.G. Shukhov, Belgorod, Russia
TYPE: Article
PAGES: from 185 to 192
STATUS: Published
LANGUAGE: Russian
KEYWORDS: ions of heavy metals, adsorption, sawdust of Acacia auriculiformis, modification
ABSTRACT (ENGLISH): A method has been developed for the purification of wastewater from ions of heavy metals using modified sawdust of Acacia auriculiformis with dilute solutions of mineral acids (HNO3, H2SO4, H3PO4) as a sorption material. The highest sorption capacity with respect to Ni2+, Cu2+, Zn2+ ions is possessed by acacia sawdust treated with 3% solutions of nitric and sulfuric acids. The values of the sorption capacity of modified sawdust with respect to heavy metal ions are approximately 1.5 times higher than those for activated carbon. A method is proposed for the purification of galvanic wastewater generated at Thien My LLC, Vinh Phuc city (Vietnam), using modified acacia sawdust as a sorption material. This method makes it possible to increase the degree of purification for heavy metal ions up to 10 times in comparison with the currently existing technology of precipitation with alkaline reagents. A basic technological scheme is proposed on the basis of the developed method, the main units of which are sorption modified with subsequent ion-exchange additional treatment in order to achieve regulatory requirements for pollutants to be purified. According to the results of biotesting using standard test objects, it was found that treated wastewater does not have a toxic effect, which leads to a decrease in anthropogenic load on the environment
ВВЕДЕНИЕ
Ионы тяжелых металлов (ИТМ), попадая в природные водоемы и водотоки со сточными водами (СВ) гальванических, сталелитейных и ряда других производств, значительно ухудшают их общее санитарное состояние, при этом оказывая токсичное и канцерогенное действие на гидробионтов. В составе промышленных СВ чаще всего встречаются ионы Cu2+, Ni2+, Zn2+ и другие. Попадая в организм человека, данные ионы вызывают функциональные расстройства нервной системы, нарушения функций печени и почек; избыток меди может вызвать болезнь Вильсона-Коновалова, а также гемолиз эритроцитов, появление гемоглобина в моче, анемию и прочее [1, 2].
Одним из наиболее эффективных и дешевых методов очистки СВ от ИТМ является адсорбционная очистка с использованием активированных углей. Вследствие высокой стоимости углей и необходимости их регенерации в последние годы активно развивается новое направление – получение и исследование сорбционных свойств материалов на основе отходов природного растительного сырья [3-9]. В ряде работ [10-12] отмечается увеличение сорбционной емкости целлюлозных сорбционных материалов (СМ) при их обработке разбавленными растворами минеральных кислот.
Деревья вида акация ушковидная (Acacia auriculiformis) (АУ) являются одними из наиболее распространенными в Юго-Восточной Азии. Древесина акации применяется для изготовления мебели, а также в качестве топлива. Отходы от переработки деревьев акации: листва, опилки, кора и другие на данный момент не находят должного применения. Обзор отечественной и зарубежной литературы показал, что в работах [13-15] содержатся результаты исследования сорбционных свойств деревьев видов Acacia nilotica, Acacia tortilis, Acacia raddiana, Acacia magnium по отношению к ионам цинка, кадмия, свинца, серебра и другим ионам. Сведения об адсорбционных характеристиках опилок АУ по отношению к ИТМ в литературе отсутствуют.
На основании вышеизложенного, целью данного исследования являлась разработка адсорбционного метода очистки СВ от ИТМ (Ni2+, Cu2+и Zn2+) с использованием в качестве СМ кислотомодифицированных опилок акации ушковидной.
ОСНОВНОЙ РАЗДЕЛ
Характеристики исходных опилок АУ представлены в таблице 1.
Таблица 1.
Характеристики исходных опилок акации ушковидной
|
№ |
Показатель |
Значение |
|
1 |
Насыпная плотность, г·см—³ |
0.15 |
|
2 |
Влажность, % |
6.93 |
|
3 |
Плавучесть, % |
25.37 |
|
4 |
Зольность, % |
0.01 |
|
5 |
Фракционный состав, %: >2 0.5-2 0.25-0.5 0.1-0.25 0.1> |
2.33 54.11 32.14 10.60 0.81 |
Адсорбционные свойства СМ в статических условиях по отношению к ИТМ определялись на модельных водных растворах солей Ni2+, Cu2+ и Zn2+ с концентрациями ионов от 10 до 1500 мг·дм-3 при дозировке СМ 10 г·дм-3. Перемешивание растворов ИТМ с исследуемым СМ осуществлялось в реакционном сосуде с использованием магнитной мешалки в течение 3 часов.
По определенным значениям начальной и конечной концентрации ИТМ в водных растворах рассчитывались адсорбционные емкости (А) опилок акации и строились изотермы адсорбции.
С целью повышения сорбционной емкости опилки акации ушковидной обрабатывались 1-3% растворами серной, азотной и фосфорной кислот. Инструментальными методами анализа исследованы физико-химические параметры нативного и модифицированных СМ. ИК спектры снимались на ИК-Фурье спектрометре марки «Avatar-360» путем таблетирования исследуемых материалов с KBr. С помощью прибора марки «Kruss DSA 20E» методом сидячей капли определены краевые углы смачивания каплей дистиллированной воды поверхности исследуемых образцов СМ. Рентгеноструктурный анализ опилок выполнялся на дифрактометре марки «Ultima IV RIGAKU». Элементный анализ материалов определялся на анализаторе марки «Vario EL». Термогравиметрический анализ (ТГА) и дифференциальная сканирующая калориметрия (ДСК) проведены на термоанализаторе марки «Simultaneous SDT Q600». Оценка величины удельной поверхности нативных и модифицированных опилок акации определялась методом низкотемпературной адсорбции-десорбции азота на приборе марки «Sorbi-MS».
Изотермы адсорбции ионов никеля, меди и цинка нативными опилками акации приведены на рисунке 1.
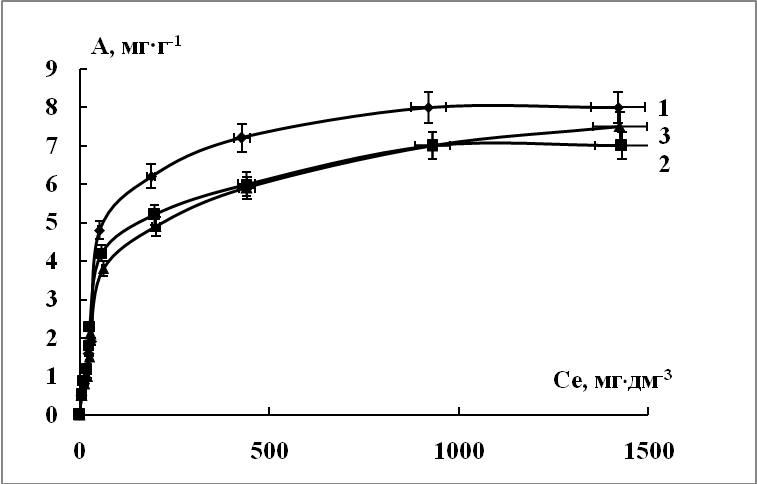
Рис. 1. Изотермы адсорбции ионов: 1 – Ni2+, 2 – Cu2+, 3 – Zn2+ опилками АУ
Аналогичным образом получены изотермы адсорбции ионов никеля, меди и цинка промышленными образцами активированного угля марки БАУ. Значения максимальных адсорбционных емкостей опилок АУ и активированного угля по отношению к исследуемым ИТМ представлены в таблице 2. По данным таблицы 2, адсорбционная емкость опилок акации по отношению к ионам Ni2+, Cu2+ и Zn2+ значительно ниже аналогичных значений для активированного угля. С целью увеличения адсорбционной емкости по отношению к ИТМ исследуемых опилок акации, проведена обработка поверхности последних растворами HNO3, H2SO4 и H3PO4 с концентрациями 1, 2 и 3 мас%. Определены адсорбционные свойства полученных модифицированных СМ по отношению к ионам Ni2+, Cu2+ и Zn2+ в статических условиях и построены изотермы адсорбции (рисунок 2).
Таблица 2.
Значения Аmax опилок акации и активированного угля по отношению к ионам никеля, меди и цинка
|
Сорбционный материал |
Сорбционная емкость А, мг·г-1 |
||
|
Ni2+ |
Cu2+ |
Zn2+ |
|
|
Опилки акации ушковидной |
8.0 |
7.0 |
7.5 |
|
Активированный уголь БАУ |
22.9 |
22.5 |
21.5 |
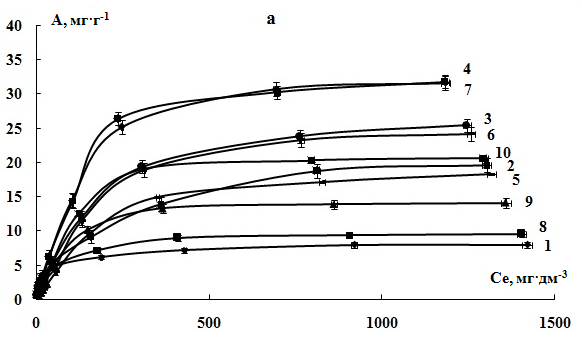
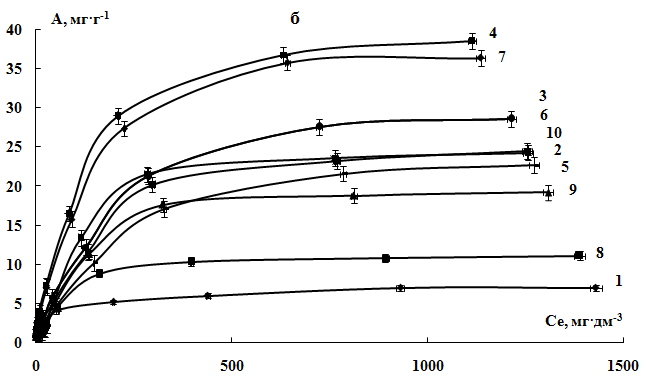
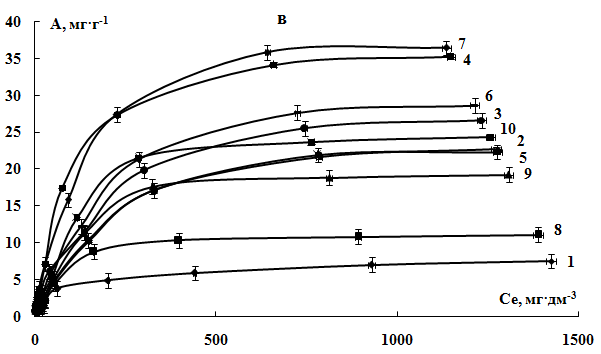
Рис. 2. Изотермы адсорбции ионов а) Ni2+, б) Cu2+, в) Zn2+: 1 – немодифицированными опилками акации и модифицированными с помощью растворов HNO3 c концентрацией: 2 – 1%, 3 – 2%, 4 – 3 %, H2SO4 с концентрацией: 5 – 1%, 6 – 2%, 7 – 3 % и H3PO4 с концентрацией: 8 – 1%,
9 – 2%, 10 – 3 %.
Представленные изотермы адсорбции исследуемых ИТМ относятся к I типу изотерм по классификации ИЮПАК и описывают мономолекулярную адсорбцию ионов на поверхности СМ.
Определены максимальные адсорбционные емкости материалов, а также, обработкой в рамках семи моделей сорбции: Ленгмюра, Фрейндлиха, Дубинина-Радушкевича, Темкина, Флори-Хаггинса, Гаркинса-Джура, Френкеля-Хелси-Хилла, получены уравнения, наиболее адекватно описывающие исследуемые процессы адсорбции, а также энергию сорбции и энергию Гиббса (табл.3).
Таблица 3.
Результаты исследования процессов сорбции ионов никеля, меди и цинка модифицированными опилками акации ушковидной
|
Сорбционный материал, опилки акации |
Ион |
A∞, мг·г-1 |
A∞, ммоль·г-1 |
Модель сорбции Уравнение процесса Коэффициент аппроксимации (R2) |
Энергия сорбции (E) Энергия Гиббса (∆G) |
|---|---|---|---|---|---|
|
До модификации |
Ni2+ |
8.0 |
0.14 |
Ленгмюра у = 9.53х + 10.06 (R2 = 0.951) |
E =1.155 кДж·моль-1 ∆G =-0.131 кДж·моль-1 |
|
Cu2+ |
7.0 |
0.11 |
Ленгмюра у = 8.88х + 10.22 (R2 = 0.976) |
E =1.175 кДж·моль-1 ∆G =-0.342 кДж·моль-1 |
|
|
Zn2+ |
7.5 |
0.12 |
Темкина у = 0.02х + 0.05 (R2 = 0.975) |
E =1.049 кДж·моль-1 ∆G =-0.783 кДж·моль-1 |
|
|
+ HNO3 (1%) |
Ni2+ |
19.6 |
0.33 |
Фрейндлиха у = 0.58х – 1.14 (R2 = 0.978) |
E =1.522 кДж·моль-1 ∆G =-1.645 кДж·моль-1 |
|
Cu2+ |
34.5 |
0.39 |
Фрейндлиха у = 0.65х – 1.10 (R2 = 0.958) |
E =1.564 кДж·моль-1 ∆G =-1.984 кДж·моль-1 |
|
|
Zn2+ |
21.0 |
0.34 |
Фрейндлиха у = 0.69х – 1.20 (R2 = 0.964) |
E =1.156 кДж·моль-1 ∆G =-0.878 кДж·моль-1 |
|
|
+ HNO3 (2%) |
Ni2+ |
25.4 |
0.43 |
Фрейндлиха у = 0.60х – 1.04 (R2 = 0.971) |
E =2.088 кДж·моль-1 ∆G =-3.534 кДж·моль-1 |
|
Cu2+ |
28.6 |
0.45 |
Фрейндлиха у = 0.60х – 1.00 (R2 = 0.968) |
E =2.285 кДж·моль-1 ∆G =-3.312 кДж·моль-1 |
|
|
Zn2+ |
25.5 |
0.41 |
Фрейндлиха у = 0.60х – 1.02 (R2 = 0.970) |
E =1.767 кДж·моль-1 ∆G =-0.199кДж·моль-1 |
|
|
+ HNO3 (3%) |
Ni2+ |
31.8 |
0.54 |
Фрейндлиха у = 0.61х – 0.90 (R2 = 0.968) |
E =2.071 кДж·моль-1 ∆G =-1.898 кДж·моль-1 |
|
Cu2+ |
38.6 |
0.61 |
Ленгмюра у = 1.70х + 3.17 (R2 = 0.994) |
E =2.438 кДж·моль-1 ∆G =-1.525 кДж·моль-1 |
|
|
Zn2+ |
35.1 |
0.54 |
Ленгмюра у = 2.43х + 3.11 (R2 = 0.994) |
E =2.035 кДж·моль-1 ∆G =-0.609 кДж·моль-1 |
|
|
+ H2SO4 (1%) |
Ni2+ |
18.3 |
0.31 |
Фрейндлиха у = 0.61х – 1.21 (R2 = 0.966) |
E =1.615 кДж·моль-1 ∆G =-2.745 кДж·моль-1 |
|
Cu2+ |
23.0 |
0.36 |
Фрейндлиха у = 0.65х – 1.17 (R2 = 0.964) |
E =1.590 кДж·моль-1 ∆G =-2.696 кДж·моль-1 |
|
|
Zn2+ |
22.7 |
0.35 |
Фрейндлиха у = 0.65х – 1.17 (R2 = 0.965) |
E =1.590 кДж·моль-1 ∆G =-2.763 кДж·моль-1 |
|
|
+ H2SO4 (2%) |
Ni2+ |
24.2 |
0.41 |
Фрейндлиха у = 0.64х – 0.09 (R2 = 0.973) |
E =1.508 кДж·моль-1 ∆G =-1.586 кДж·моль-1 |
|
Cu2+ |
28.8 |
0.45 |
Фрейндлиха у = 0.60х – 1.00 (R2 = 0.968) |
E =2.285 кДж·моль-1 ∆G =-3.312 кДж·моль-1 |
|
|
Zn2+ |
28.6 |
0.44 |
Фрейндлиха у = 0.60х – 1.00 (R2 = 0.968) |
E =2.403 кДж·моль-1 ∆G =-3.459 кДж·моль-1 |
|
|
+ H2SO4 (3%) |
Ni2+ |
31.6 |
0.54 |
Ленгмюра у = 2.37х + 4.84 (R2 = 0.974) |
E =2.090 кДж·моль-1 ∆G =-1.746 кДж·моль-1 |
|
Cu2+ |
36.5 |
0.57 |
Флори-Хаггинса у = -3.72х – 2.38 (R2 = 0.992) |
E =2.403 кДж·моль-1 ∆G =-3.402 кДж·моль-1 |
|
|
Zn2+ |
36.4 |
0.56 |
Флори-Хаггинса у = -3.72х — 2.37 (R2 = 0.992) |
E =2.403 кДж·моль-1 ∆G =-3.459 кДж·моль-1 |
|
|
+ H3PO4 (1%) |
Ni2+ |
9.6 |
0.16 |
Темкина у = 0.03х + 0.08 (R2 = 0.928) |
E =1.293 кДж·моль-1 ∆G =-0.355 кДж/моль-1 |
|
Cu2+ |
11.1 |
0.17 |
Ленгмюра у = 6.41х + 10.09 (R2 = 0.950) |
E =1.270 кДж·моль-1 ∆G =-1.103 кДж·моль-1 |
|
|
Zn2+ |
11.1 |
0.17 |
Темкина у = 0.03х + 0.08 (R2 = 0.928) |
E =1.729 кДж·моль-1 ∆G =-3.225 кДж·моль-1 |
|
|
+ H3PO4 (2%) |
Ni2+ |
14.1 |
0.24 |
Темкина у = 0.05х + 0.11 (R2 = 0.950) |
E =1.335 кДж·моль-1 ∆G =-0.883 кДж·моль-1 |
|
Cu2+ |
19.2 |
0.30 |
Фрейндлиха у = 0.59х – 1.12 (R2 = 0.959) |
E =1.533 кДж·моль-1 ∆G =-1.667 кДж·моль-1 |
|
|
Zn2+ |
18.9 |
0.29 |
Фрейндлиха у = 0.56х – 1.11 (R2 = 0.958) |
E =2.156 кДж·моль-1 ∆G =-4.085 кДж·моль-1 |
|
|
+ H3PO4 (3%) |
Ni2+ |
20.6 |
0.35 |
Ленгмюра у = 3.16х + 4.89 (R2 = 0.985) |
E =1.898кДж·моль-1 ∆G =-1.061 кДж·моль-1 |
|
Cu2+ |
24.3 |
0.38 |
Фрейндлиха у = 0.56х – 0.98 (R2 = 0.966) |
E =2.070 кДж·моль-1 ∆G =-2.468 кДж·моль-1 |
|
|
Zn2+ |
24.0 |
0.37 |
Фрейндлиха у = 0.52х – 0.97 (R2 = 0.966) |
E =3.053 кДж·моль-1 ∆G =-5.939 кДж·моль-1 |
Обработка опилок акации растворами кислот приводит к увеличению их адсорбционной емкости по исследуемым ИТМ. При этом эффект от модификации увеличивается в ряду кислот: H3PO4 < H2SO4 = HNO3. Наибольшей адсорбционной емкостью по отношению к ионам Ni2+, Cu2+ и Zn2+ обладают опилки, обработанные 3% растворами азотной (А∞ = 31.8, 38.6 и 35.1 мг·г-1 соответственно) и серной кислот (А∞ = 31.6, 36.5 и 36.4 мг·г-1 соответственно). Значения адсорбционной емкости модифицированных опилок акации ушковидной по отношению к ИТМ примерно в 1.5 раза превышают аналогичные значения для активированного угля. Термодинамические параметры процессов (энергия адсорбции и энергия Гиббса) указывают на протекание самопроизвольной физической адсорбции при данной температуре (298 К).
Термодинамические параметры (энергия сорбции и энергия Гиббса) указывают на то, что протекает самопроизвольная физическая адсорбция.
Процесс адсорбции ионов никеля и меди нативными опилками акации лучше всего описывается моделью Ленгмюра, а ионов цинка − моделью Темкина. Модификация опилок акации растворами минеральных кислот приводит к образованию неравномерно распределенных участков с большей энергией сорбции по данным ионам (модель Фрейндлиха).
В некоторых случаях (опилки-HNO3 (3%) по отношению к меди, опилки-H2SO4 (3%) и опилки-H3PO4 (3%) по отношению к никелю), наблюдается равномерная модификация всей поверхности сорбционного материала (модель Ленгмюра).
На основании вышеизложенного, инструментальными методами анализа исследованы структурные и поверхностные параметры нативного СМ и модифицированного H2SO4, как наиболее эффективным и доступным реагентом. Первоначально определялось влияние обработки опилок акации 3% раствором H2SO4 на их элементный состав (табл. 4).
Таблица 4.
Элементный состав нативных и модифицированных опилок акации ушковидной
|
Наименование образца |
Содержание элемента, % |
|||
|
С |
H |
N |
O и другие элементы |
|
|
Нативные опилки |
48.39 |
5.77 |
0.32 |
45.52 |
|
Опилки, обработанные 3% раствором H2SO4 |
43.53 |
5.39 |
0.31 |
50.77 |
По данным таблицы 4 показано незначительное снижение массовой доли углерода, водорода и азота в модифицированном образце. Увеличение содержания кислорода свидетельствует об увеличении количества гидрофильных групп в структуре СМ и, соответственно, увеличении адсорбционной емкости по ИТМ.
В подтверждение вышесказанного методом сидячей капли определено, что обработка древесины 3% раствором H2SO4, краевой угол смачивания снижается с 71.8о до 59.5о.
Незначительные изменения ИК-спектров опилок Acacia auriculiformis до и после обработки 3% раствором H2SO4 наблюдаются в диапазоне 2950–2800 и 1457 см-1, при 1507, 1734, 1383, 1056, ~ 900 и 3412 см-1, что может свидетельствовать об извлечении низкомолекулярных фрагментов биополимеров, входящих в состав опилок, в раствор в процессе воздействия 3% раствора H2SO4.
Обработка опилок раствором H2SO4 приводит к упорядочению структуры и увеличению кристалличности с 0,19 до 0,23.
Увеличение кристалличности происходит вследствие деструкции межмолекулярных связей в ходе гидролиза. Гидролитической деструкции подвергаются связи гемицеллюлоз с лигнином и целлюлозой. Это способствует образованию более пористой структуры и увеличению удельной поверхности материала.
Установлено, что после кислотной обработки удельная поверхность материала возрастает от 8,6 м2·г-1 до 20.6 м2·г-1, что больше первоначального значения в 2,4 раза.
В дальнейшей работе очистке подвергали СВ гальванического производства предприятия ООО «Тхиен Ми» (Thien My). При изготовлении бытовой техники, мототехники и различных запасных частей на предприятии применяют противокоррозионную обработку, в ходе которой образуются гальваностоки, содержащие ионы Cu2+, Ni2+ и Zn2+. Объем гальваностоков предприятия составляет примерно 45 м3·сут-1. Средние концентрации в СВ за период 2016-2018 гг. по ионам меди составили 280-505 мг·дм-3, по ионам никеля ‑ 1.2-3.2 мг·дм-3, по ионам цинка‑ 90.2-120 мг·дм-3.
СВ после гальванических ванн объединяются в одном реакторе, в который добавляется 5%-ный водный свежеприготовленный Ca(OH)2 до значения рН = 8-11 и образования малорастворимых гидроксидов никеля, меди и цинка. после добавления к сточной воде флокулянта, седиментации и обезвоживания осадок направляется в шламонакопитель. После корректировки рН очищенная сточная вода сбрасывается в реку Фан. При этом концентрация ионам Cu2+ составила 0.030-1.490 мг·дм-3, ионов Ni2+ ‑ 0.021-1.910 мг·дм-3, ионов Zn2+ ‑0.054-2.105 мг·дм-3.
Недостатком существующей на предприятии технологии является образование большого количества гальваношлама.
Для очистки реальных гальваностоков с использованием в качестве СМ опилок АУ, обработанных 3% раствором H2SO4, СВ ООО «Тхиен Ми» в объеме 20 дм3 помещались в аппарат с мешалкой, куда добавлялись сернокислотномодифицированные опилки АУ. Начальные концентрации ИТМ составили: по ионам Cu2+ – 398 мг·дм-3, по ионам Ni2+ – 2.2 мг·дм-3, по ионам Zn2+ – 99.78 мг·дм-3, дозировка СМ – 20 г·дм-3, температура – 25 оС, время адсорбции – 3 ч. По окончании данного промежутка времени, сорбционный материал извлекался фильтрованием, высушивался, а в очищенной сточной воде определялись остаточные концентрации меди, никеля и цинка составили соответственно: 2.03, 0.4 и менее 0.02 мг·дм-3. Эффективность удаления составила: по ионам Cu(II) − 99%, Ni(II) − 81% и Zn(II) − 99.9% соответственно. Для доведения значений концентраций меди и никеля до допустимых значений, рассмотрена возможность доочистки гальваностоков с использованием ионообменной смолы марки «Lewatit Monoplus TP 207». Для этого в стеклянные колонки диаметром 20 мм загружалось 10 г названной ионообменной смолы, через которые пропускалось 500 см3 гальванических СВ, предварительно прошедших адсорбционную очистку. Остаточная концентрация ионов меди, никеля и цинка, после очистки, составила 0.05, 0.01 и 0.002 мг/дм3 соответственно. Остаточные концентрации ИТМ намного ниже требуемых значений, что позволяет сбрасывать доочищенные СВ в реку Фан (song Phan).
На основании проведенных испытаний по сжиганию отработанного СМ по данным ТГА показано, что убыль массы образца более 99% происходит при температуре 463оС.
С целью количественной экологической оценки предлагаемого технологического решения проведено биотестирование очищенных гальваностоков. В результате адсорбции коэффициент разбавления пробы воды, при котором достигается 50% смертность стандартных тест объектов Paramecium caudatum и Daphnia magna снижается с 74712 раз до 36.6 раз, а после ионного обмена − до 1 раз. Таким образом, конечным продуктам является нетоксичная вода, не оказывающая негативного воздействия на экосистему реки Phan.
ВЫВОДЫ
Изучены адсорбционные свойства нативных и модифицированных опилок акации ушковидной по отношению к ионам никеля, меди и цинка в статических условиях. Построены изотермы адсорбции, определены уравнения и термодинамические параметры процессов. Установлено, что обработка опилок акации слабоконцентрированными растворами минеральных кислот (HNO3, H2SO4 и H3PO4) способствует увеличению сорбционной емкости по отношению к ИТМ. Наибольшей адсорбционной емкостью по ионам Ni2+, Cu2+ и Zn2+ (в 1.5 раза превышающие аналогичных значений для активированного угля) обладают опилки акации, обработанные 3% растворами азотной и серной кислот. Методами элементного анализа, ИК-спектроскопии, рентгенофазового анализа, адсорбции-десорбции азота и другими методами определено, что обработка поверхности опилок разбавленными растворами минеральных кислот приводит к увеличению гидрофильности и кристалличности образцов, а также образованию более развитой поверхности, что может быть обусловлено вымыванием низкомолекулярных органических соединений − продуктов кислотного гидролиза соединений, входящих в состав опилок акации ушковидной. Проведена апробация модифицированных опилок акации по очистке реальных СВ − в условиях предприятия ООО «Тхиен Ми» (Вьетнам). В результате адсорбционной очистки образующихся СВ с последующей доочисткой на ионообменной смоле, содержание ИТМ на выходе намного ниже нормативных значений, что позволяет сбрасывать доочищенные СВ в реку Фан. Отработанные опилки акации предлагается утилизировать сжиганием при температуре выше 463оС. Биотестирование очищенных гальваностоков с использованием стандартных тест объектов Paramecium caudatum и Daphnia magna указывает на то, что конечным продуктом является нетоксичная вода, не оказывающая негативного воздействия на экосистему реки Phan.
Материал подготовлен при поддержке центра высоких технологий БГТУ им. В.Г. Шухова.
ЛИТЕРАТУРА
1. Ma, J. Heavy metal removal from aqueous solutions by calcium silicate powder from waste coal fly-ash / J. Ma, G. Qin, Y. Zhang, J. Sun, S. Wang, L. Jiang // Journal of Cleaner Production. ‒ 2018. ‒ V. 182. ‒ P. 776-782.
2. Mugera, G.W. The potential of ball-milled south african bentonite clay for attenuation of heavy metals from acidic wastewaters: simultaneous sorption of Co2+, Cu2+, Ni2+, Pb2+, and Zn2+ ions / G.W. Mugera, M. Vhahangwele // Journal of Environmental Chemical Engineering. ‒ 2015. ‒ V. 3. ‒ № 4. ‒ P. 2416-2425.
3. Saeed, A. Removal and recovery of lead(II) from single and multimetal (Cd, Cu, Ni, Zn) solutions by crop milling waste (Black gram husk) / A. Saeed, M. Iqbal, M.W. Akhtar // Journal of Hazardous Materials. ‒ 2005. ‒ V. 117. ‒ № 1. ‒ P. 65-73.
4. Krishnani, K.K. Biosorption mechanism of nine different heavy metals onto biomatrix from rice husk / K.K. Krishnani, X. Meng, C. Christodoulatos, V.M. Boddu // Journal of Hazardous Materials. ‒ 2008. ‒ V. 153. ‒ № 3. ‒ P. 1222-1234.
5. Guiza, S. Biosorption of heavy metal from aqueous solution using cellulosic waste orange peel / S. Guiza // Ecological Engineering. ‒ 2017. ‒ V. 99. ‒ P. 134-140.
6. Chakraborty, R. Adsorption of heavy metal ions by various low-cost adsorbents: a review / R. Chakraborty, A. Asthana, A.K. Singh, B. Jain, A.B.H. Susan // International Journal of Environmental Analytical Chemistry. ‒ 2020. ‒ 39 p.
7. Sverguzova, S.V. Using wastes of buckwheat processing as sorption materials for the removal of pollutants from aqueous media: a review / S.V. Sverguzova, I.G. Shaikhiev, R.Z. Galimova, A.S. Grechina // IOP Conference Series: Materials Science and Engineering. ‒ 2020. ‒ Vol. 945. ‒ № 012044. ‒ 11 p.
8. Shaikhiev, I.G. Using cucurbits by-products as reagents for disposal of pollutants from water environments (a literature review) / I.G. Shaikhiev, N.V. Kraysman, S.V. Sverguzova // Biointerface Research in Applied Chemistry. ‒ 2021. ‒ vol. 11. ‒ No 5. ‒ P. 12689-12705.
9. Shaikhiev, I.G. Onion (Allium Cepa) processing waste as a sorption material for removing pollutants from aqueous media / I.G. Shaikhiev, N.V. Kraysman, S.V. Sverguzova // Biointerface Research in Applied Chemistry. ‒ 2022. ‒ vol. 12. ‒ No 3. ‒ P. 3173-3185.
10. Denisova, T.R. Investigation of phenol adsorption on barley husk modified by low — concentrated sulfuric acid solutions / T.R. Denisova, R.Z. Galimova, I.R. Nizameev, I.G. Shaikhiev, G.V. Mavrin // Journal of Fundamental and Applied Sci ences. ‒ 2017. ‒ V. 9. ‒ P. 1480-1490.
11. Zolgharnein, J.Crossed mixture process design optimization and adsorption characterization of multimetal (Cu(II), Zn(II) and Ni(II)) removal by modified Buxus sempervirens tree leaves / J. Zolgharnein, M. Bagtash, S. Feshki, P. Zolgharnein, D. Hammond // Journal of the Taiwan Institute of Chemical Engineers. ‒ 2017. ‒ V. 78. ‒ P. 104-117.
12. Li, X.M. Removal of Pb (II) from aqueous solutions by adsorption onto modified areca waste: kinetic and thermodynamic studies / X.M. Li, W. Zheng, D.B. Wang, Q. Yang, J.B. Cao, X. Yue, T.T. Shen, G.M. Zeng // Desalination. ‒ 2010. ‒ V. 258. ‒ № 1-3. ‒ P. 148-153.
13. Rani, N. Removal of Cr (VI) from Aqueous Solutions by Acacia nilotica Bark / N. Rani, A. Gupta, A.K. Yadav // Environmental Technology. ‒ 2006. ‒ V. 27. ‒ № 6. ‒ P. 597-602.
14. Khabibi, J. Reducing hazardous heavy metal ions using mangium bark waste / J. Khabibi, W. Syafii, R.K. Sari // Environmental Science and Pollution Research. ‒ 2016. ‒ V. 23. ‒ № 16. ‒ P. 16631-16640.
15. Kumar, S. Removal of fluoride by thermally activated carbon prepared from neem (Azadirachta indica) and kikar (Acacia arabica) leaves / S. Kumar, A. Gupta, J.P. Yadav // Journal of Environmental Biology. ‒ 2008. ‒ V. 29. ‒ № 2. ‒ P. 227-232.
